เขียนโดย รศ.นพ.ภาวิน พัวพรพงษ์
ความหมาย
ภาวะอุ้งเชิงกรานอักเสบ? หรือ? pelvic? inflammatory? disease? (PID)? หมายถึง? ภาวะการอักเสบและติดเชื้อของอวัยวะสืบพันธุ์ส่วนบนในสตรี? โดยทั่วไปได้แก่? มดลูก? ท่อนำไข่? รังไข่? และอวัยวะข้างเคียงในอุ้งเชิงกราน 1 ?จะเห็นว่า? มีความหมายค่อนข้างกว้างในกรณีที่ทราบว่า? มีการอักเสบและติดเชื้อของอวัยวะใดอวัยวะหนึ่งแน่ชัด? อาจใช้คำที่มีความหมายจำเพาะ? เช่น? การอักเสบของมดลูก (metritis)? การอักเสบของท่อนำไข่ (salpingitis)? การอักเสบของรังไข่? (oophoritis) เป็นต้น? แต่อย่างไรก็ตาม? ภาวะอุ้งเชิงกรานอักเสบ? ส่วนใหญ่มักจะวินิจฉัยจากอาการทางคลินิก? จึงมักใช้คำกว้าง ๆ? หรือมีความหมายโดยรวมมากกว่า
ภาวะอุ้งเชิงกรานอักเสบ? อาจแบ่งชนิดตามระยะเวลาที่เป็น? ได้แก่? ชนิดเฉียบพลัน? (acute? pelvic? inflammatory? disease)? และชนิดเรื้อรัง? (chronic? pelvic? inflammatory? disease)? โดยระยะเวลาที่จะวินิจฉัยว่าเป็นชนิดเรื้อรังไม่ได้มีการกำหนดชัดเจน? แต่อาจดูจากการได้รับการวินิจฉัยเกิน? 2? ครั้งภายในปีเดียวกัน? ส่วนใหญ่สาเหตุของภาวะอุ้งเชิงกรานอักเสบชนิดเรื้อรังมักเป็นผลต่อเนื่องจากการรักษาอุ้งเชิงกรานอักเสบชนิดเฉียบพลันอย่างไม่ถูกต้องหรือไม่เพียงพอ
อุบัติการณ์และความสำคัญ
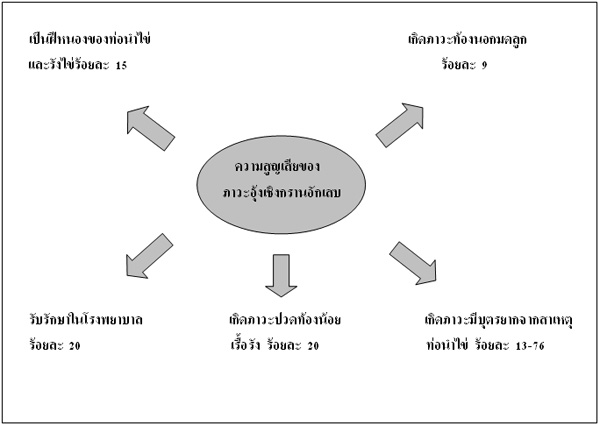
อุบัติการณ์ของภาวะอุ้งเชิงกรานอักเสบ? ยังไม่ทราบแน่ชัด? เนื่องจากการวินิจฉัยส่วนใหญ่ได้จากอาการทางคลินิก? โดยการวินิจฉัยที่ถือว่าเป็นการวินิจฉัยที่แน่ชัดและเป็นมาตรฐาน? (gold? standard)? ได้แก่? การตรวจโดยใช้การเจาะส่องกล้องตรวจทางหน้าท้อง? (laparoscopy) 1??เป็นวิธีการวินิจฉัยที่มีความยุ่งยากและผู้ป่วยจะต้องได้รับการผ่าตัด? จึงไม่ใช้โดยทั่วไปทางคลินิกเป็นวิธีแรก? จะใช้ในกรณีที่มีปัญหาในการวินิจฉัยหรือในการวิจัย? ในประเทศสหรัฐอเมริกาในแต่ละปี? จะมีสตรีราวหนึ่งล้านคนที่มีภาวะอุ้งเชิงกรานอักเสบ? โดยร้อยละ? 20? ของผู้ป่วยเหล่านี้? จำเป็นจะต้องนอนในโรงพยาบาล 2??ร้อยละ? 20? เกิดภาวะปวดท้องน้อยเรื้อรัง 1??ร้อยละ? 15? จะกลายเป็นฝีหนองของท่อนำไข่และรังไข่? (tuboovarian? abscess)??2?และคาดคะเนว่าร้อยละ? 9-10? ของสตรีที่มีภาวะอุ้งเชิงกรานอักเสบจะมีภาวะท้องนอกมดลูก? (ectopic? pregnancy)??1, 3นอกจากนี้ยังทำให้เกิดภาวะมีบุตร ยากจากสาเหตุของท่อนำไข่ร้อยละ? 13-76? ขึ้นอยู่กับความรุนแรงและจำนวนครั้งที่เป็น4, 5???ทำให้ต้องเสียค่าใช้จ่ายจำนวนมากในการแก้ไขภาวะแทรกซ้อนนี้? สรุปดังรูปที่ 1??? สำหรับในประเทศอังกฤษ? พบความชุกของภาวะอุ้งเชิงกรานอักเสบร้อยละ? 1.76?? ในประเทศไทยยังไม่มีการรวบรวมข้อมูลและรายงานที่ชัดเจน? แต่คาดว่าตัวเลขน่าจะสูง? อย่างไรก็ตามตัวเลขที่รายงานโดยทั่วไปจะต่ำกว่าความเป็นจริง? เนื่องจากผู้ป่วยส่วนหนึ่งจะไม่มีอาการหรือมีอาการน้อยแล้วไม่ได้มารับการรักษา? จึงน่าจะมีการรายงานน้อยกว่าความเป็นจริง
รูปที่? 1?? แสดงความสูญเสียของภาวะอุ้งเชิงกรานอักเสบ
สาเหตุและพยาธิกำเนิด
ภาวะอุ้งเชิงกรานอักเสบเป็นกลุ่มอาการทางคลินิกที่เกิดจากการผ่านของเชื้อโรคจากอวัยวะสืบพันธุ์สตรีส่วนล่างขึ้นมาในอวัยวะสืบพันธุ์สตรีส่วนบนโดยนับตั้งแต่ผ่านเข้ามาที่มดลูก? ซึ่งจะทำให้เกิดการอักเสบและติดเชื้อในอุ้งเชิงกรานตามมา? เชื้อโรคที่ทำให้เกิดภาวะอุ้งเชิงกรานอักเสบได้แก่? ?mycoplasma, เชื้อโรคทั่วไปที่อยู่ในช่องคลอดทั้งชนิด? anaerobic? และ? aerobic, aerobic? streptococci, Mycobacterium ?tuberculosis? และที่พบเป็นสาเหตุนำได้บ่อยคือ? เชื้อที่ทำให้เกิดโรคติดต่อทางเพศสัมพันธ์? ได้แก่? Chalmydia? trachomatis? และ? Neisseria? gonorrhoeae 7??การลุกล้ำของเชื้อโรคอาจไปตาม? muscosal? surface? ตามช่องว่างระหว่างเซลล์ ( intercellular? space )? หรือ? ตามตัวอสุจิขึ้นไป? 8, 9??ขึ้นอยู่กับลักษณะของเชื้อแต่ละชนิด? การติดเชื้อดังกล่าวจะก่อให้เกิดอาการอักเสบ? มีเม็ดเลือดขาวมากขึ้น? และมีการหลั่งเอ็นไซม์จาก? lysosome? ทำให้เกิดการตายของเนื้อเยื่อ? เกิดหนองในท่อนำไข่? รังไข่? หรือในอุ้งเชิงกราน? สิ่งแวดล้อมในอุ้งเชิงกรานเปลี่ยนแปลงเป็นเหตุชักนำให้เกิดการติดเชื้อจากเชื้อโรคหลายชนิดได้
ชนิดของเชื้อโรคที่เป็นสาเหตุของภาวะอุ้งเชิงกรานอักเสบจะมีความหลากหลาย? ตามแต่ลักษณะของประชากรในแต่ละประเทศ? หรือทวีป? และตามแต่ละช่วงเวลา? ในสหรัฐอเมริกาพบสาเหตุของภาวะอุ้งเชิงกรานอักเสบเป็น? Chlamydia? trachomatis? ตั้งแต่ร้อยละ? 14-65? ในอังกฤษพบสาเหตุจาก? Chlamydia? trachomatis? ร้อยละ? 39-40? สาเหตุจาก? Neisseria? gonorrhoeae? ร้อยละ? 143?ยังไม่มีข้อมูลรายงานในประเทศไทยซึ่งจะต้องมีการศึกษาต่อไป? ปัจจุบันแนวโน้มของสาเหตุของภาวะอุ้งเชิงกรานอักเสบมักพบ? Chlamydia? trachomatis? สูงขึ้น?? เนื่องจากเมื่อมีการติดเชื้อและอักเสบของอวัยวะสืบพันธ์ส่วนล่าง? อาการทางคลินิกมักไม่ชัดเจนเหมือนสาเหตุจาก? Neisseria? gonorrhoeae? จึงทำให้มาทำการตรวจรักษาล่าช้า? โอกาสจะเกิดการติดเชื้อขึ้นไปถึงส่วนบนจึงสูงกว่า
ภาวะแทรกซ้อนของภาวะอุ้งเชิงกรานอักเสบที่พบได้แก่? ภาวะท้องนอกมดลูก? ภาวะมีบุตรยากจากสาเหตุท่อนำไข่? (tubal? factor? infertility)? และอาการปวดท้องน้อยเรื้อรัง? (chromic? pelvic? pain)? นอกจากนี้ยังพบว่าภาวะนี้มีความสัมพันธ์กับความเสี่ยงของมะเร็งรังไข่ที่สูงขึ้น? ?10??พยาธิกำเนิดของภาวะแทรกซ้อนเหล่านี้ยังมีความซับซ้อนขึ้นอยู่กับหลายปัจจัย? ได้แก่? พันธุกรรม? ภูมิคุ้มกัน? และความรุนแรงของเชื้อ? ปัจจุบันพบว่าการเกิดภาวะอุ้งเชิงกรานอักเสบและการทำลายของเยื่อบุท่อนำไข่จากการติดเชื้อ? Chlamydia? trachomatis? เกิดจากมี? delayed? hypersensivity? reaction? ต่อ Chlamydial? heat? shock? protein? (HSP-60)? 60 Kda? ซึ่งเป็นโปรตีนของเชื้อ? Chlamydia? trachomatis?? ?สำหรับปัจจัยเรื่องภูมิคุ้มกันพบว่า? ในผู้ป่วยโรคเอดส์ที่มีอาการ? หรือผู้ที่มีภูมิคุ้มกันบกพร่องจะพบภาวะอุ้งเชิงกรานอักเสบมีอาการทางคลินิกรุนแรงกว่าและระยะเวลาของโรคยาวนานกว่า
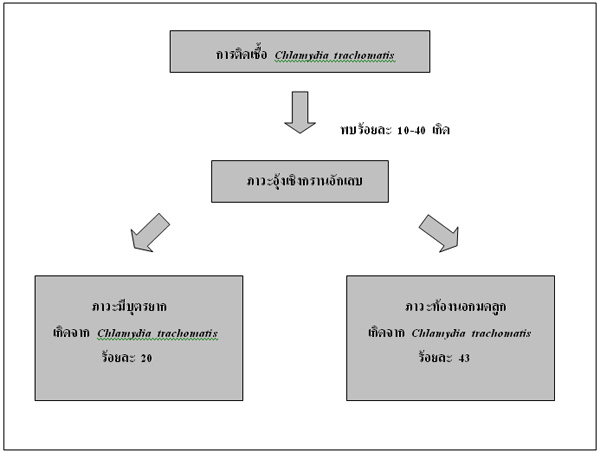
การติดเชื้อ? Chlamydia? trachomatis? พบร้อยละ? 10-40?11? ที่ก่อให้เกิดภาวะอุ้งเชิงกรานอักเสบ? ความเสี่ยงของการเกิดภาวะแทรกซ้อนขึ้นอยู่กับจำนวนครั้งของการเกิดภาวะอุ้งเชิงกรานอักเสบ? ความเสี่ยงของการเกิดภาวะท้องนอกมดลูกและการมีบุตรยากจากสาเหตุของท่อนำไข่หลังจากเกิดภาวะอุ้งเชิงกรานอักเสบ 1? ครั้ง มี? odd? ratio? เท่ากับ? 6? และเกิด? 2? ครั้ง มี? odd? ratio? เท่ากับ? 17??12?จากการศึกษาในหนูพบว่า? ภาวะอุ้งเชิงกรานอักเสบสามารถเกิดได้ภายใน? 5? วัน? หลังการติดเชื้อ? Chlamydia? trachomatis? ดังนั้นหากไม่สามารถเริ่มต้นการรักษาภายใน? 3? วันหลังเริ่มอาการปวดท้องน้อยจะมีความเสี่ยงต่อการเกิดภาวะอุ้งเชิงกรานอักเสบและภาวะมีบุตรยากสูงขึ้นถึง? 3? เท่า? การให้การวินิจฉัยที่ถูกต้องตั้งแต่แรกเริ่มจึงเป็นสิ่งที่จำเป็น? การติดเชื้อ? Chlamydia? trachomatis? พบเป็นสาเหตุของการมีบุตรยากร้อยละ? 20? และสาเหตุของการเกิดภาวะท้องนอกมดลูกร้อยละ? 433? สรุปดังรูปที่ 2
รูปที่? 2?? ?? แสดงผลแทรกซ้อนจาการติดเชื้อ? Chlamydia? trachomatis
การศึกษาอุบัติการณ์ของภาวะแทรกซ้อนจากภาวะอุ้งเชิงกรานอักเสบมีความลำบาก? เนื่องจากต้องอาศัยกลุ่มตัวอย่างที่มีจำนวนมากและต้องติดตามผลเป็นเวลานาน? โดยเฉพาะอย่างยิ่งการศึกษาความชุกของภาวะมีบุตรยากจากภาวะอุ้งเชิงกรานอักเสบ? เนื่องจากจะได้รับข้อมูลเพียงจากผู้ที่ต้องการมีบุตรเท่านั้น? อย่างไรก็ตาม? จากข้อมูลที่ได้มีการศึกษาพบว่าหญิงที่มีประวัติมีภาวะอุ้งเชิงกรานอักเสบจะมีความเสี่ยงต่อการเกิดภาวะท้องนอกมดลูกสูงขึ้น? 6? เท่า? และเสี่ยงต่อการเกิดภาวะมีบุตรยากจากสาเหตุของท่อนำไข่สูงขึ้น? 14? เท่า? เทียบกับหญิงทั่วไป?12??สำหรับข้อมูลเรื่องการป้องกันภาวะแทรกซ้อนเหล่านี้จะกล่าวในรายละเอียดต่อไป
ปัจจัยส่งเสริม
การทราบปัจจัยส่งเสริมหรือปัจจัยเสี่ยงต่อการเกิดภาวะอุ้งเชิงกรานอักเสบ? จะสามารถทำให้เกิดการวางแผนยุทธศาสตร์การป้องกันและลดภาวะอุ้งเชิงกรานอักเสบลงได้? ปัจจัยส่งเสริมของภาวะอุ้งเชิงกรานอักเสบมีดังนี้
1. ?อุปนิสัยในเรื่องเพศสัมพันธ์?? ได้แก่? อายุที่มีเพศสัมพันธ์ครั้งแรก? จำนวนของคู่นอนตลอดในช่วงชีวิต? ความถี่ของการเปลี่ยนคู่นอน? และการมีเพศสัมพันธ์โดยไม่มีการป้องกัน?13? อุปนิสัยเหล่านี้ขึ้นอยู่กับลักษณะเศรษฐกิจ? สังคม? ศาสนา? และวัฒนธรรมแต่ละพื้นที่ด้วย
2. ?อายุ? สตรีที่มีอายุน้อย? คือ? 16-24? ปี? มีแนวโน้มจะเกิดโรคติดต่อทางเพศสัมพันธ์สูงกว่าในกลุ่มอายุที่สูงขึ้น? อาจเป็นเนื่องจากโอกาสที่ผู้รับเชื้อจะเป็นโรคง่าย? (susceptibility)? เนื่องจากความเข้มข้นของ? protective? chlamydial? antibodies? ที่ต่ำกว่า??? ปากมดลูกปลิ้นออก? (larger? cervical? ectopy) มากกว่า???? เชื้อสามารถผ่านมูกบริเวณปากมดลูกง่ายกว่า? (greater? permeability? of? cervical? mucus) จึงทำให้เกิดภาวะอุ้งเชิงกรานอักเสบมากกว่า13-15
3.? การคุมกำเนิด? มีรายละเอียดแต่ละชนิดดังนี้
-? การใส่ห่วงอนามัย? จาก? meta ? analysis? รวบรวม? 36? การศึกษาพบว่ามีความเสี่ยงเพิ่มขึ้น? 3.3? เท่า? คือ relative? risk? 3.3? (95 % CI? 2.1 to 5.3 )??16, 17?แต่ความเสี่ยงนี้พบแค่ใน? 2-3? สัปดาห์แรกหลังการใส่ห่วงอนามัยเท่านั้น ?17, 18
– การรับประทานยาคุมกำเนิด? มีแนวโน้มว่าจะช่วยป้องกันภาวะอุ้งเชิงกรานอักเสบจากการที่ยาเม็ดคุมกำเนิดทำให้มูกบริเวณปากมดลูกข้นขึ้น?19??แต่การศึกษา? PEACH? study? ยังไม่ยืนยันข้อมูลนี้20?
– การคุมกำเนิดโดยวิธีขวางกั้น? (barrier method) และการใช้ยาฆ่าเชื้ออสุจิ? จะช่วยป้องกันและลดการเกิดภาวะอุ้งเชิงกรานอักเสบได้?20??โดยขัดขวางพยาธิกำเนิดดังกล่าวข้างต้น
4.? ประวัติการเป็นโรคติดต่อทางเพศสัมพันธ์? โดยเฉพาะอย่างยิ่งการติดเชื้อ? Neisseria gonorrhoeae? และ Chlamydia? trachomatis? หากไม่ได้รับการรักษาที่ถูกต้อง? โรคอาจลุกลามเกิดภาวะอุ้งเชิงกรานอักเสบได้21?
5.? การสูบบุหรี่? สัมพันธ์กับการเพิ่มความเสี่ยงต่อการเกิดภาวะอุ้งเชิงกรานอักเสบ? โดยสาเหตุเกิดจากระบบภูมิคุ้มกันที่ลดน้อยลงหรือผลกระทบต่อระดับฮอร์โมนเอสโตรเจน? นอกจากนี้การสูบบุหรี่ยังสะท้อนถึงพฤติกรรมเสี่ยงอื่นในกลุ่มประชากรที่มีเศรษฐานะต่ำด้วย?22, 23?
6.? การสวนล้างช่องคลอด ?(douching)? สัมพันธ์กับภาวะอุ้งเชิงกรานอักเสบโดยเปลี่ยนแปลงสิ่งแวดล้อมและชะล้างแบคทีเรียประจำถิ่น(normal flora)ที่อยู่ในช่องคลอด? แต่ละประเทศมีลักษณะวัฒนธรรมที่แตกต่างกัน? ในสหรัฐอเมริการพบสตรีมีการสวนล้างช่วยคลอดมากกว่าในประเทศอังกฤษ?3, 24?
7.? การทำหัตถการในโพรงมดลูก? ได้แก่? การตรวจ? hysterosalpingography?25??การขูดมดลูก? การทำแท้ง?26??การทำหัตถการเหล่านี้เพิ่มโอกาสที่เชื้อโรคจะลุกล้ำขึ้นไปในอวัยวะสืบพันธุ์ส่วนบนและเกิดภาวะอุ้งเชิงกรานอักเสบได้
ลักษณะทางคลินิกและสิ่งตรวจพบ 16, 27
อาการและอาการแสดงของผู้ป่วยที่มีภาวะอุ้งเชิงกรานอักเสบมีได้ตั้งแต่ไม่พบอาการจนกระทั่งถึงมีอาการหนักและชัดเจนมากทั้งนี้ขึ้นอยู่กับชนิดและความรุนแรงของเชื้อ? ระยะเวลาที่เป็น? และการรักษาที่ได้รับมาก่อน? โดยทั่วไป? อาการปวดท้องน้อยเป็นอาการที่พบได้บ่อยที่สุดในผู้ป่วยที่มีภาวะอุ้งเชิงกรานอักเสบ? ลักษณะอาการปวดท้องน้อยจะปวดทั่วไปทั้งสองด้านโดยไม่จำเป็นจะต้องปวดรุนแรงมาก? ส่วนอาการร่วมอื่นๆ มักขึ้นอยู่กับชนิดของการติดเชื้อ? สำหรับการติดเชื้อ? Neisseria? gonorrhoeae? และ? Chlamydia? trachomatis? อาจพบผู้ป่วยมีอาการตกขาวที่ผิดปกติ? ปัสสาวะแสบขัด? (dysuria)? ปัสสาวะบ่อย และกลั้นปัสสาวะไม่ได้
(frequency? and? urgency)? ในกรณีที่ผู้ป่วยรับประทานยาคุมกำเนิด? หรือหลังการทำแท้ง? อาจพบอาการเลือดออกผิดปกติ? (persistent? vaginal? spotting)? สำหรับกรณีที่โรคลุกลามขึ้นไปในอุ้งเชิงกรานอาจพบอาการทาง? systemic? ได้แก่? ไข้? คลื่นไส้? อาเจียน? ร่วมด้วย
สำหรับอาการแสดงและการตรวจทางห้องปฏิบัติการที่ตรวจพบได้แก่? ตกขาว(vaginal discharge)ผิดปกติหรือมีมูกปนหนองจากปากมดลูก? หากนำตกขาวไปส่องกล้องจุลทรรศน์ จะพบลักษณะของเม็ดเลือดขาวชนิด? polymorphonuclear? เป็นจำนวนมาก (พบสัดส่วนของเม็ดเลือดขาวต่อเซลล์เยื่อบุผนังช่องคลอดในสัดส่วนมากกว่า? 1 : 1)? หากใช้ไม้พันสำลีเช็ดมูกบริเวณปากมดลูกจะมองเห็นสีเหลืองหรือเหลืองปนเขียวของมูก? เช่นเดียวกัน? หากส่องกล้องจุลทรรศน์ดูมูกจะพบเม็ดเลือดขาวชนิด? polymorphonuclear? มากกว่า? 30? เซลล์ ต่อ oil? immersion? field? ในผู้ป่วยที่มีอาการปวดท้อง? จะตรวจพบการกดเจ็บบริเวณปีกมดลูกทั้งสองด้านและเจ็บเมื่อมีการโยกปากมดลูก? (cervical? motion? tenderness)? อาการอื่น ๆ ที่แสดงอาการอักเสบและการติดเชื้อที่ตรวจพบได้คือ? การมีไข้และหากเจาะเลือดตรวจจะพบ? leukocytosis ?มี? erythrocyte? sedimentation? rate และ? C-reactive? protein ?สูงขึ้น ในกรณีที่มีอาการรุนแรง อาจคลำได้พบก้อนกดเจ็บบริเวณปีกมดลูกด้วย บางรายหากมี ?cul? de? sac? โป่ง? เจาะ? culdocentesis? จะพบหนอง? หากมีการส่งตรวจเพาะเชื้อจากอวัยวะสืบพันธุ์ส่วนล่างและพบ? Neisseria? gonorrhoeae? หรือ? Chlamydia? trachomatis? จะช่วยในการวินิจฉัยภาวะอุ้งเชิงกรานอักเสบด้วย
การตรวจ? endometrial? biopsy? สามารถให้การวินิจฉัย? endometritis? โดยใช้? Pipelle? endometrial? suction? curette? ทำการ? biopsy?? ชิ้นเนื้อในโพรงมดลูก? หัตถการนี้สามารถทำในคลินิกหรือห้องฉุกเฉินได้? เกณฑ์การวินิจฉัยใช้การตรวจพบ neutrophil มากกว่า? 5? ตัว? ใน? 400? fields? ของ? endometrial ?surface? epithelium? หรือพบ plasma? cell มากกว่า? 1 ตัว? ใน? 120? fields? ของ? endometrial? stroma
การใช้คลื่นเสียงความถี่สูงตรวจผ่านทางช่องคลอด(transvaginal ultrasound;TVS)ในกรณีที่มีภาวะอุ้งเชิงกรานอักเสบรุนแรงจะพบมีหนองใน? cul? de? sac? หรือมีก้อนฝีหนองของท่อนำไข่และรังไข่? การใช้? power? Doppler? ช่วยให้การตรวจวินิจฉัยดีขึ้น? โดยมีการวัด? blood? flow? เพื่อแสดงภาวะ? hyperemia? ของการอักเสบของท่อนำไข่? สำหรับการใช้? magnetic? resonance? imaging(MRI)? เชื่อว่ามีประสิทธิภาพสูงแต่ข้อมูลในการใช้ยังมีจำกัด
การใช้การเจาะส่องกล้องตรวจทางหน้าท้อง? (laparoscopy)? ใช้เกณฑ์การวินิจฉัยดังนี้
– ?เกณฑ์ขั้นต่ำ? จะต้องพบ? hyperemia? ของผิวของท่อนำไข่? การรวมของผนังท่อนำไข่และการมีexudate? เหนียวอยู่บนผิวของท่อนำไข่บริเวณปลาย? fimbria? หากไม่มีภาวะท่อตัน
– ?การจัดแบ่งความรุนแรง? แบ่งเป็น
1. ความรุนแรงน้อย (mild)? มีลักษณะตามเกณฑ์ขั้นต่ำ? ร่วมกับ? ท่อนำไข่เคลื่อนไหวได้อิสระและไม่ตัน? อาจพบ? exudate? เหนียวบนท่อนำไข่ร่วมด้วย
2. ความรุนแรงปานกลาง? (moderate)? จะมีการอักเสบมากขึ้นกว่า? พบมี? fibrin? เกาะติดบริเวณผิวserosa? ของท่อนำไข่? ท่อนำไข่เริ่มติดโดยมีพังผืดหลวม ๆ ยึด
3.?ความรุนแรงมาก? (severe)? พบบริเวณ? peritoneum? มี? congestion? มาก? มีพังผืดยึดอวัยวะในอุ้งเชิงกราน? และพบ? pyosalpinx? หรือ? ก้อนฝีหนองของท่อนำไข่และรังไข่
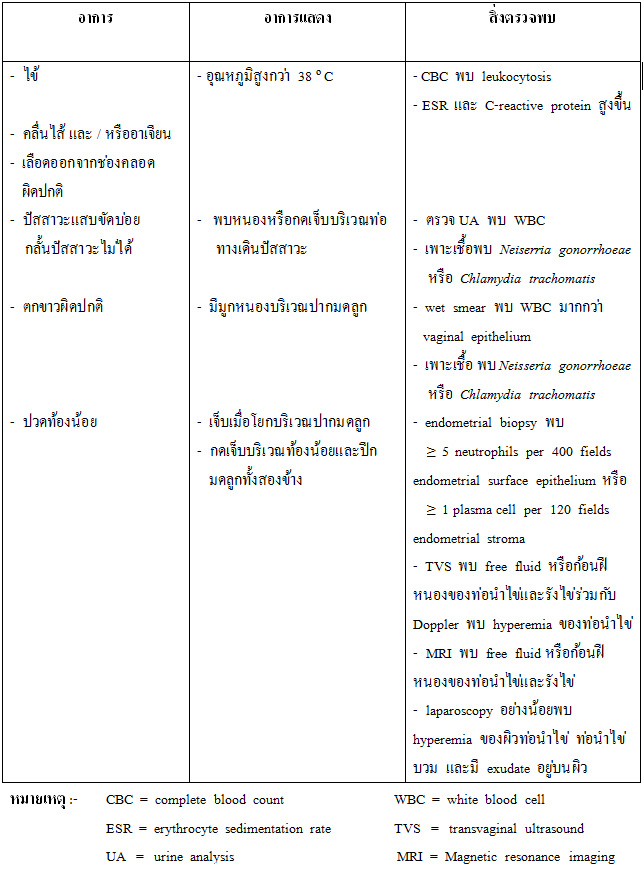
รายละเอียดของความสามารถในการแยกโรคและความจำเพาะจะกล่าวต่อไปในหัวข้อการวินิจฉัย?สำหรับลักษณะทางคลินิกและส่งตรวจพบสรุปดังตารางที่? 1
ตารางที่? 1 ?อาการ? อาการแสดง? และสิ่งตรวจพบในภาวะอุ้งเชิงกรานอักเสบ
การวินิจฉัย
การวินิจฉัยภาวะอุ้งเชิงกรานอักเสบมีความลำบากเนื่องจากความหลากหลายของอาการตั้งแต่ไม่มีอาการหรือมีอาการเล็กน้อยไปจนถึงมีอาการรุนแรง? เกณฑ์ทางคลินิกที่ใช้ในการวินิจฉัยก็มีหลากหลาย? และมีความสามารถในการวินิจฉัยโรคได้มากน้อยไม่เท่ากัน? การใช้อาการแสดงทางคลินิกได้แก่? การกดเจ็บบริเวณปีกมดลูก? มี? sensitivity? สูงคือ? ร้อยละ? 96? แต่มี? specificity? ต่ำ? คือร้อยละ? 4?16??หากใช้อาการแสดง? การกดเจ็บบริเวณปีกมดลูกร่วมกับการเจ็บเมื่อโยกปากมดลูก? sensitivity? จะลดลงเหลือร้อยละ? 83? และ? specificity? เพิ่มขึ้นเป็นร้อยละ22? 16? ดังนั้นจึงควรใช้เกณฑ์หลายข้อในการวินิจฉัยภาวะอุ้งเชิงกรานอักเสบ? โดยทั่วไปการใช้เกณฑ์การวินิจฉัยทางคลินิกจะมี? sensitivity? และ? specificity? ประมาณร้อยละ? 50 16?และมี? positive? predictive? value? ร้อยละ? 65-90 ?28เทียบกับการเจาะส่องกล้องตรวจทางหน้า?? ปัจจุบัน? CDC? (Centers? for? Disease? Control )?28?มีการปรับปรุงเกณฑ์การวินิจฉัยเพิ่มเติม? ในปี? 2002? เพื่อเพิ่มประสิทธิภาพในการวินิจฉัยแยกโรค ดังนี้
เกณฑ์การวินิจฉัยขั้นต่ำ? (minimal? criteria)
- มีกดเจ็บบริเวณมดลูกหรือปีกมดลูก
- เจ็บเมื่อโยกบริเวณปากมดลูก
เกณฑ์เสริมการวินิจฉัย? (additional? criteria)
- มีไข้โดยการวัดอุณหภูมิทางปากมากกว่า? 38.3 ? C
- มี? discharge? เป็นมูกปนหนอง? ( mucopurulent )? จากช่องคลอดหรือปากมดลูก
- มี? white? blood? cell? จากการส่องกล้องจุลทรรศน์? ตรวจ? wet? smear? ของ? discharge จากช่องคลอด
- Erythrocyte? sedimentation? rate (ESR) สูงขึ้น
- C-reactive? protein? สูงขึ้น
- ตรวจทางห้องปฏิบัติการพบการติดเชื้อ Neisseria? gonorrhoeae? หรือ ?Chlamydia? trachomatis? ทางปากมดลูก
เกณฑ์ที่จำเพาะในการวินิจฉัย? ( specific? criteria)
- endometrial? biopsy? พบหลักฐานทางพยาธิวิทยาของเยื่อบุโพรงมดลูกอักเสบ (endometritis)
- การตรวจคลื่นเสียงความถี่สูงผ่านทางช่องคลอด หรือ? magnetic? resonance? imaging? (MRI)? พบท่อนำไข่หนา? มีของเหลวอยู่ภายใน? อาจจะพบ? free? pelvic? fluid? หรือ? การยึดเกาะของท่อนำไข่และรังไข่เป็นก้อน? (tubo-ovarian? complex)
- ลักษณะของการเจาะส่องกล้องตรวจทางหน้าท้องเข้าได้กับภาวะอุ้งเชิงกรานอักเสบ
ในการวินิจฉัยจะต้องมีเกณฑ์ขั้นต่ำครบ? สำหรับเกณฑ์เสริมการวินิจฉัยและเกณฑ์ที่จำเพาะในการวินิจฉัย? หากพบเพิ่มขึ้นจะช่วยเพิ่มความจำเพาะในการวินิจฉัยโรค
ความสามารถในการวินิจฉัยโรคของเกณฑ์จำเพาะในการวินิจฉัยแต่ละข้อนั้น? พบว่า? endometrial? biopsy? มี? sensitivity? ร้อยละ? 89, specificity? ร้อยละ? 67,? positive? predictive? value? ร้อยละ? 84? และ? negative? predictive? value? ร้อยละ? 100?16??? การตรวจ? MRI? พบมี? sensitivity? ร้อยละ? 95? และ? specificity? ร้อยละ? 89?16? การเจาะส่องกล้องตรวจทางหน้าท้องถือเป็นการตรวจที่เป็นมาตรฐานการวินิจฉัยที่แน่ชัด (gold? standard)? เปรียบเทียบกับวิธีอื่น ๆ?????? อย่างไรก็ตาม? การตรวจวินิจฉัยด้วยวิธีการเหล่านี้? ไม่แพร่หลาย? เนื่องจากใช้เวลาและลำบากในการตรวจ? ใช้เครื่องมือเทคโนโลยีในการตรวจ? และความสามารถของผู้ตรวจและการแปลผล? ดังนั้นปัจจุบันส่วนใหญ่การให้การวินิจฉัยยังคงใช้อาการและอาการแสดงทางคลินิกร่วมกับการตรวจทางห้องปฏิบัติการเบื้องต้นเป็นหลัก? ซึ่งปัญหาในการให้การวินิจฉัยที่แน่ชัดจึงมีอยู่มาก? อนาคตมีความพยายามจะหาการตรวจทางห้องปฏิบัติการที่ทำได้ง่าย? แปลผลได้รวดเร็ว? และมีความถูกต้องสูง? โดยมีความพยายามศึกษา? interleukin-6? ซึ่งเป็นสารที่พบเมื่อเกิดการอักเสบ? และพบว่ามีระดับสูงทั้งใน? discharge? จากช่องคลอดและในกระแสเลือดเมื่อมีภาวะอุ้งเชิงกรานอักเสบ? ?29?การตรวจ? interleukin-6? ตรวจแปลผลได้ใน? 2-3? ชั่วโมง? หากมีการวิจัยศึกษาเพิ่มเติมถึง? sensitivity? และ? specificity? อาจนำมาใช้ช่วยในการวินิจฉัยภาวะอุ้งเชิงกรานอักเสบได้ดีและสะดวกมากขึ้น
การรักษา
หลักในการรักษาภาวะอุ้งเชิงกรานอักเสบ? คือ? การให้การรักษาด้วยยาปฏิชีวนะที่ครอบคลุมเชื้อที่เป็นสาเหตุ? โดยทั่วไปการเกิดภาวะอุ้งเชิงกรานอักเสบในระยะท้ายของโรคมักเกิดจากการติดเชื้อหลายชนิด? ยาที่ให้จึงควรเลือกอย่างเหมาะสม? ในการรักษาสามารถแบ่งเป็น? การรักษาแบบผู้ป่วยนอกและการรักษาแบบผู้ป่วยใน? ตามข้อแนะนำของ? CDC? 2002??28 ดังนี้
1.การรักษาแบบผู้ป่วยนอก? มักใช้ในกรณีอาการของโรคไม่รุนแรง? ผู้ป่วยร่วมมือในการรักษาดีและตอบสนองต่อยาดี? ไม่มีข้อสงสัยในการวินิจฉัย? ชนิดของยาที่ใช้สามารถเลือกได้ดังนี้

สูตรทางเลือกอื่น ๆ
มีข้อมูลจากการศึกษารายงานที่อาจจะสามารถใช้? amoxicilin / clavulanic? acid? ร่วมกับ? การใช้? doxycycline? ได้
หมายเหตุ???????? สำหรับการรักษาแบบผู้ป่วยนอกนี้? ผู้ป่วยควรได้รับการนัดเพื่อติดตามการตอบสนองของโรคใน? 72? ชั่วโมง ?ของการรักษา???? หากอาการไม่ดีขึ้น? แนะนำให้ทำการรักษาแบบผู้ป่วยใน
2.?การรักษาแบบผู้ป่วยใน? มักใช้ในกรณีที่อาการของโรครุนแรงหรืออาจพิจารณาตามข้อบ่งชี้ของ? CDC? 2002??28 ?ดังนี้
-? สงสัยมีภาวะฉุกเฉินที่ต้องได้รับการผ่าตัด? เช่น? ภาวะไส้ติ่งอักเสบ? ภาวะท้องนอกมดลูก? ถุงน้ำรังไข่แตก
-? ผู้ป่วยตั้งครรภ์
-? ผู้ป่วยไม่ตอบสนองทางคลินิกต่อการรักษาด้วยยาชนิดรับประทาน
-? ผู้ป่วยไม่สามารถทนรับการรักษาหรือติดตามการรักษาโดยสูตรยาแบบผู้ป่วยนอกได้
-? ผู้ป่วยที่มีอาการของโรครุนแรง? คลื่นไส้? อาเจียน? มีไข้สูง
-? ผู้ป่วยที่มีก้อนหนองบริเวณท่อนำไข่และรังไข่
สำหรับข้อบ่งชี้บางอย่าง? ได้แก่? ผู้ป่วยวัยรุ่น? ผู้ป่วยอายุมากกว่า? 35? ปี? หรือ? ผู้ป่วยติดเชื้อไวรัส?เอดส์? ยังไม่มีข้อมูลยืนยันถึงประโยชน์ชัดเจนที่ได้รับจากการรับการรักษาแบบผู้ป่วยใน
ชนิดของสูตรยา สำหรับการรักษาแบบผู้ป่วยใน? มีดังนี้
ในสูตรยา? Regimen A และ B? หลังให้ครบ? 24? ชั่วโมงหากผู้ป่วยมีลักษณะอาการทางคลินิกดีขึ้น? สามารถเปลี่ยนยาเป็นชนิดรับประทาน? โดยให้? doxycycline? 100? mg? รับประทานวันละ? 2? ครั้งเป็นเวลา? 14? วัน? และอาจพิจารณาให้? clindamycin? หรือ? metronidazole? รับประทานร่วมด้วยในกรณีที่สงสัยว่าอาจจะมีก้อนหนองในท่อนำไข่และรังไข่
สูตรทางเลือกอื่น ๆ
– ofloxacin? 400? mg? ฉีดเข้าหลอดเลือดดำทุก? 12? ชั่วโมง? หรือ
– levofloxacin? 500? mg? ฉีดเข้าหลอดเลือดดำ? วันละครั้ง
โดยอาจพิจารณายาเหล่านี้ร่วมด้วยหรือไม่ก็ได้
– metronidazole? 500 mg? ฉีดเข้าหลอดเลือดดำทุก? 8? ชั่วโมง? หรือ
– ?ampicillin / sulbactam? 3 g? ฉีดเข้าหลอดเลือดดำทุก? 6? ชั่วโมง
ร่วมกับ
– doxycyclin? 100? mg ?รับประทานหรือฉีดเข้าหลอดเลือดดำทุก? 12? ชั่วโมงได้มีการเปรียบเทียบความคุ้มค่าในการรักษาแบบผู้ป่วยนอกและผู้ป่วยใน? ในผู้ป่วยที่มีความรุนแรงของโรคตั้งแต่เล็กน้อยถึงปานกลาง? พบว่า? ไม่มีความแตกต่างในด้านผลการรักษา ได้แก่? อัตราการตั้งครรภ์? ภาวะมีบุตรยาก? ภาวะปวดท้องน้อยเรื้อรัง? และภาวะท้องนอกมดลูก30?
ในการรักษาภาวะอุ้งเชิงกรานอักเสบนั้น? นอกจากการดูแลรักษาโดยยาปฏิชีวนะแล้วยังมีการดูแลด้านอื่น ๆ ร่วมด้วยได้แก่
– ?การให้ผู้ป่วยนอนท่า? Fowler?s? position? โดยหวังว่าจะให้หนองและการติดเชื้อในช่องท้องจำกัดอยู่ในส่วนล่างของอุ้งเชิงกราน
– ?การให้ยาแก้ปวด? ยาลดไข้? บรรเทาอาการ
– ?การให้น้ำเกลือทางหลอดเลือด? ในรายที่มีอาการคลื่นไส้อาเจียนมาก? รับประทานอาหารไม่ได้
-?ที่สำคัญ? คือ? การติดตามคู่นอนผู้ป่วยมาตรวจรักษา? โดยแนะนำให้ทำการรักษาด้วยยาปฏิชีวนะที่
ครอบคลุมเชื้อ? Neisseria? gonorrheae? และ? Chlamydia? trachomatis? เพราะพบบ่อยที่คู่นอนมีการติดเชื้อและไม่มีอาการ? ?28ปัญหาเหล่านี้เป็นปัญหาที่มักจะถูกละเลยจึงควรให้ควรใส่ใจเป็นอย่างมาก
ภาวะแทรกซ้อน
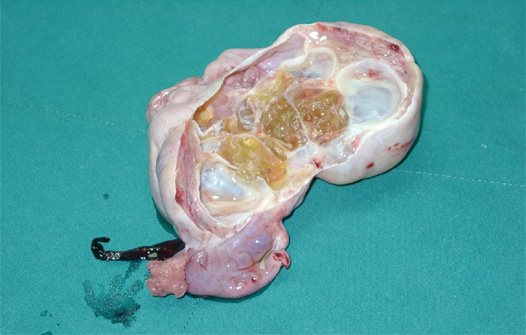
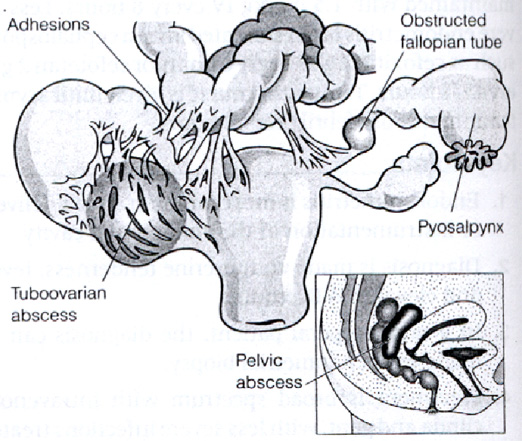
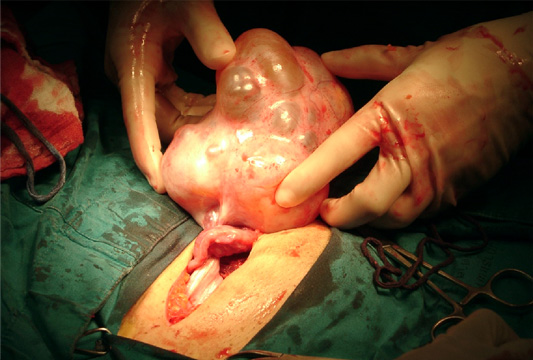
1.?ก้อนฝีหนองของท่อนำไข่และรังไข่? (tubo-ovarian? abscess? หรือ? TOA)? พบภาวะแทรกซ้อนนี้
ได้ร้อยละ? 15??2, 27??? พยาธิสรีรวิทยา? คล้ายคลึงกับการเกิดภาวะอุ้งเชิงกรานอักเสบแต่มีการติดเชื้อเข้าไปในส่วนของ? ovarian? stroma? ทำให้เกิดการทำลายเนื้อของรังไข่? และเกิดโพรงหนอง? หรืออาจพบเป็นก้อนหนองระหว่างอวัยวะในอุ้งเชิงกรานก็ได้? เช่น? ภายในหรือระหว่างท่อนำไข่? รังไข่? และมดลูก? บางกรณีอาจพบส่วนของลำไส้เข้ามายึดติดเป็นส่วนหนึ่งของผนังของก้อนฝีหนอง
การวินิจฉัยภาวะแทรกซ้อนนี้? เริ่มตั้งแต่มีประวัติของอาการภาวะอุ้งเชิงกรานอักเสบ? ตรวจร่างกายพบก้อนบริเวณปีกมดลูก? การตรวจเพิ่มเติมเพื่อการวินิจฉัย? ได้แก่? การตรวจคลื่นเสียงความถี่สูง? การเอกซเรย์คอมพิวเตอร์? (CT? scan)?? และการตรวจ? MRI? ซึ่งอาจจะพบหนองในท่อนำไข่และรังไข่? หรือเป็นก้อนหนองระหว่างอวัยวะที่มีพังผืดยึดในอุ้งเชิงกราน
การรักษาคล้ายคลึงกับภาวะอุ้งเชิงกรานอักเสบ? แต่หากภายใน? 72? ชั่วโมง? ผู้ป่วยไม่ตอบสนองต่อการรักษา? หรือสงสัยมีการแตกของก้อนฝีหนอง? ควรทำการเปิดผ่าตัดช่องท้อง? โดยพิจารณาทำการระบายหนองออกและอาจทำร่วมกับการตัดปีกมดลูกข้างนั้นออกในกรณีที่ผู้ป่วยยังต้องการมีบุตรอยู่? หรือ? ผ่าตัดมดลูกและปีกมดลูกทั้งสองข้างออกในกรณีที่ไม่ต้องการมีบุตรแล้วหรือมีอาการติดเชื้อในกระแสเลือดอย่างรุนแรงเป็นอันตรายต่อชีวิต? 27??ปัจจุบันมีการใช้การตรวจคลื่นเสียงความถี่สูงผ่านทางช่องคลอดและทางทวารหนักเจาะดูดหนองออกจากก้อนฝีหนองโดยสามารถทำได้อย่างปลอดภัย? และลดความจำเป็นในการผ่าตัดเปิดหน้าท้องลงได้?31, 32
2.? ภาวะมีบุตรยากจากสาเหตุท่อนำไข่? เป็นผลจากมีการอักเสบและถูกทำลายของท่อนำไข่? จำนวนครั้งของการเกิดภาวะอุ้งเชิงกรานอักเสบจะเพิ่มความเสี่ยงต่อการเกิดภาวะมีบุตรยาก? โดยอัตราการเกิดการมีบุตรยากหลังการเกิดภาวะอุ้งเชิงกรานอักเสบรุนแรง? 1? ครั้งเท่ากับร้อยละ ?27? ในกรณีเกิด? 3? ครั้ง? หรือมากกว่า? ความเสี่ยงนี้จะเพิ่มขึ้นร้อยละ 50-6027?(โดยทั่วไปอัตราการเกิดภาวะมีบุตรยากจากสาเหตุของท่อนำไข่พบร้อยละ? 13-76? ขึ้นอยู่กับความรุนแรงและจำนวนครั้งที่เกิดภาวะอุ้งเชิงกรานอักเสบ4, 5)? การพยากรณ์โรคเรื่องภาวะมีบุตรยากไม่ปรากฏว่าสัมพันธ์กับชนิดของเชื้อที่ทำให้เกิดภาวะอุ้งเชิงกรานอักเสบ27?? ภาวะนี้โดยทั่วไปจะทำให้ต้องเสียค่าใช้จ่ายเป็นจำนวนมากในการรักษาโดยใช้เทคโนโลยีการเจริญพันธุ์? และเพิ่มความสูญเสียทางเศรษฐกิจของประเทศ
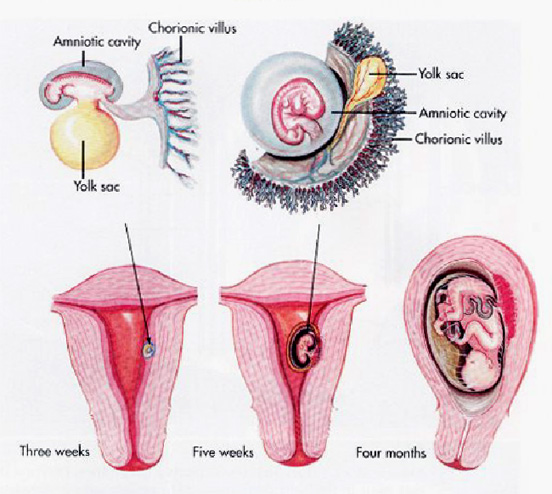
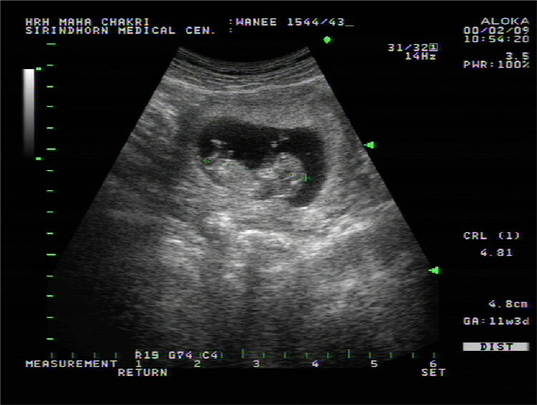
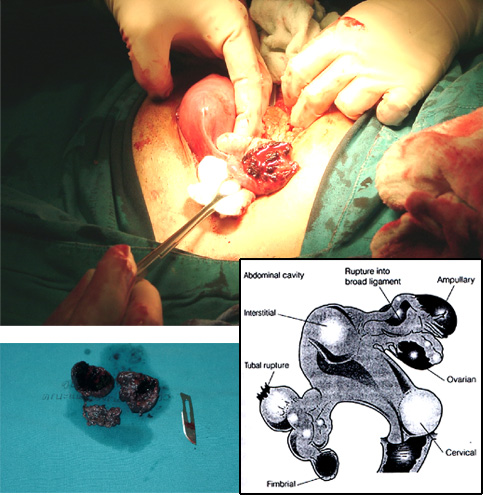
3.? ภาวะท้องนอกมดลูก? เช่นเดียวกัน? เนื่องจากมีการทำลายท่อนำไข่? หากเกิดการปฏิสนธิได้? ก็จะเกิดการขัดขวางการเดินทางของไข่ที่ปฏิสนธิแล้วมาฝังตัวในโพรงมดลูก เกิดภาวะท้องนอกมดลูก? ผู้ป่วยที่มีภาวะอุ้งเชิงกรานอักเสบจะมีความเสี่ยงต่อการเกิดภาวะนี้เพิ่มขึ้น? 4-6? เท่า? หรือคิดเป็นร้อยละ? 9-10 1,3, 27?
4.?ภาวะปวดท้องน้อยเรื้อรัง? พบร้อยละ? 20? ของผู้ที่มีประวัติอุ้งเชิงกรานอักเสบ? สาเหตุการเกิดเชื่อว่าเกิดจากการมีพังผืดในอุ้งเชิงกราน? หรือการมี? hydrosalpinx? โดยจะพบปัญหาเรื่องการมีความเจ็บปวดขณะมีเพศสัมพันธ์สูงมากกว่าครึ่งหนึ่งของผู้ป่วยที่มีภาวะปวดท้องน้อยเรื้อรังด้วย1, 27?
5.? ภาวะอุ้งเชิงกรานอักเสบซ้ำ? พบร้อยละ? 25 โดยโครงสร้างของท่อนำไข่ที่ผิดปกติไป? จะเพิ่มความเสี่ยงของการติดเชื้อ? และผู้ป่วยที่มีภาวะอุ้งเชิงกรานอักเสบก็มีแนวโน้มจะเกิดการติดเชื้อซ้ำจากเชื้อเดิมที่ติดเชื้อในครั้งแรกสูงขึ้น?27
6.? Fitz-Hugh-Cutis syndrome? เป็นความผิดปกติที่เกิดจากการมีพังผืดเป็นเส้นกั้นระหว่างตับและผนังหน้าท้องทางด้านหน้า (violin-string adhesion)? โดยจะพบอาการ ของ? perihepatitis? ซึ่งกลุ่มอาการนี้จะสัมพันธ์กับการติดเชื้อในอุ้งเชิงกรานและมีพังผืดยึดรอบตับ? (perihepatic adhesion)? โดยการติดเชื้อที่เป็นสาเหตุเป็นได้ทั้ง? Neiserria? gonorrhoeae? และ? Chlamydia? trachomatis? ?ความรุนแรงของกลุ่มอาการนี้สัมพันธ์กับความรุนแรงของการเกิดพังผืดในอุ้งเชิงกรานภายหลังเกิดภาวะอุ้งเชิงกรานอักเสบ? ในกรณีที่มีอาการเจ็บชายโครงขวาเรื้อรัง? การรักษาจำเป็นต้องเจาะส่องกล้องผ่านหน้าท้องเพื่อไปเลาะตัดพังผืดบริเวณรอบ ๆ ตับ?27
การป้องกัน
1. ป้องกันและควบคุมโรคติดต่อทางเพศสัมพันธ์? ?โดยการให้ความรู้เรื่องโรค? วิธีการคุมกำเนิด??????? วิธีการป้องกัน? และการใช้ถุงยางอนามัย?? ร่วมกับกระตุ้นให้มีการตื่นตัวและรณรงค์เรื่องการป้องกันโรค?? การตรวจคัดกรองและการรักษาผู้ป่วยที่มีมูกหนองบริเวณปากมดลูก? หรือเสี่ยงต่อการติดเชื้อ? ?Neisseria? gonorrhoeae? หรือ? Chlamydia? trachomatis? อย่างเหมาะสม? โดยเน้นความใส่ใจในเรื่องการติดตามและการตรวจรักษาคู่นอนของผู้ป่วย
2. ?ปรับเปลี่ยนค่านิยม? และอุปนิสัยเรื่องเพศสัมพันธ์? เพื่อลดพฤติกรรมเสี่ยง
3. กระตุ้นแพทย์ให้เห็นความสำคัญของภาวะอุ้งเชิงกรานอักเสบ? และความสูญเสียที่เกิดขึ้นจากภาวะแทรกซ้อน? เพื่อให้ใส่ใจในการวินิจฉัยแต่แรกเริ่มและเพียงพอเหมาะสม
4. ในการทำหัตถการต่าง ๆ ของแพทย์? ควรใส่ใจเรื่องเทคนิคการปราศจากเชื้อ? ( Sterile? technique)?เพื่อลดความเสี่ยงในการเกิดภาวะอุ้งเชิงกรานอักเสบ
?
สำหรับการศึกษาต่อไป จะเห็นว่า ยังมีปัญหาอีกมากมาย ได้แก่? การสร้างคำนิยามของภาวะอุ้งเชิงกรานอักเสบทางระบาดวิทยา?? การศึกษาปัจจัยทางสังคม? พฤติกรรมและประชากรวิทยาที่เกี่ยวข้องกับภาวะอุ้งเชิงกรานอักเสบเพิ่มเติม??? การศึกษาความชุกและอุบัติการณ์ของภาวะอุ้งเชิงกรานอักเสบ?? การพัฒนาการตรวจคัดกรองโรคในหน่วยดูแลสุขภาพปฐมภูมิ??? การสร้าง? ?clinical practice guideline ในการให้การวินิจฉัยและการดูแลรักษาภาวะอุ้งเชิงกรานอักเสบ ??การรณรงค์ต่าง ๆ ถึงผลในการป้องกันและควบคุมโรค? หากได้รับการสนใจศึกษาวิจัยอย่างเป็นระบบจะทำให้ลดภาวะอุ้งเชิงกรานอักเสบและภาวะแทรกซ้อนในอนาคตลงได้
หนังสืออ้างอิง
1. Ross J. Pelvic inflammatory disease. Bmj 2001; 322:658-9.
2. McNeeley SG, Hendrix SL, Mazzoni MM, Kmak DC, Ransom SB. Medically sound, cost-effective treatment for pelvic inflammatory disease and tuboovarian abscess. Am J Obstet Gynecol 1998; 178:1272-8.
3. Simms I, Stephenson JM. Pelvic inflammatory disease epidemiology: what do we know and what do we need to know? Sex Transm Infect 2000; 76:80-7.
4. Aral SO, Cates W, Jr. The increasing concern with infertility. Why now? Jama 1983; 250:2327-31.
5. Cates W, Farley TM, Rowe PJ. Worldwide patterns of infertility: is Africa different? Lancet 1985; 2:596-8.
6. Simms I, Rogers P, Charlett A. The rate of diagnosis and demography of pelvic inflammatory disease in general practice: England and Wales. Int J STD AIDS 1999; 10:448-51.
7. Sweet R. Microbial etiology of pelvic inflammatory disease. In: Lander D, Sweet R, ed. Pelvic inflammatory disease. New? York: Springer-Verlag, 1996:12-5.
8. Soper DE. Pelvic inflammatory disease. Infect Dis Clin North Am 1994; 8:821-40.
9.??????? Leiva JL, Peterson EM, Wetkowski M, de la Maza LM, Stone SC. Microorganisms in semen used for artificial insemination. Obstet Gynecol 1985; 65:669-72.
10. Risch HA, Howe GR. Pelvic inflammatory disease and the risk of epithelial ovarian cancer. Cancer Epidemiol Biomarkers Prev 1995; 4:447-51.
11. Stamm WE, Guinan ME, Johnson C, Starcher T, Holmes KK, McCormack WM. Effect of treatment regimens for Neisseria gonorrhoeae on simultaneous infection with Chlamydia trachomatis. N Engl J Med 1984; 310:545-9.
12. Westrom LV. Sexually transmitted diseases and infertility. Sex Transm Dis 1994; 21:S32-7.
13. Washington AE, Aral SO, Wolner-hanssen P, Grimes DA, Holmes KK. Assessing risk for pelvic inflammatory disease and its sequelae. Jama 1991; 266:2581-6.
14. Westrom L. Incidence, prevalence, and trends of acute pelvic inflammatory disease and its consequences in industrialized countries. Am J Obstet Gynecol 1980; 138:880-92.
15. Cates W, Jr., Rolfs RT, Jr., Aral SO. Sexually transmitted diseases, pelvic inflammatory disease, and infertility: an epidemiologic update. Epidemiol Rev 1990; 12:199-220.
16. Ross JD. An update on pelvic inflammatory disease. Sex Transm Infect 2002; 78:18-9.
17. Gareen IF, Greenland S, Morgenstern H. Intrauterine devices and pelvic inflammatory disease: meta-analyses of published studies, 1974-1990. Epidemiology 2000; 11:589-97.
18. Lee NC, Rubin GL, Borucki R. The intrauterine device and pelvic inflammatory disease revisited: new results from the Women’s Health Study. Obstet Gynecol 1988; 72:1-6.
19. Panser LA, Phipps WR. Type of oral contraceptive in relation to acute, initial episodes of pelvic inflammatory disease. Contraception 1991; 43:91-9.
20. Ness RB, Soper DE, Holley RL, et al. Hormonal and barrier contraception and risk of upper genital tract disease in the PID Evaluation and Clinical Health (PEACH) study. Am J Obstet Gynecol 2001; 185:121-7.
21. Padian NS, Washington AE. Pelvic inflammatory disease. A brief overview. Ann Epidemiol 1994; 4:128-32.
22. Hersey P, Prendergast D, Edwards A. Effects of cigarette smoking on the immune system. Follow-up studies in normal subjects after cessation of smoking. Med J Aust 1983; 2:425-9.
23. Pasley JN, Rank RG, Hough AJ, Jr., Cohen C, Barron AL. Effects of various doses of estradiol on chlamydial genital infection in ovariectomized guinea pigs. Sex Transm Dis 1985; 12:8-13.
24. Scholes D, Daling JR, Stergachis A, Weiss NS, Wang SP, Grayston JT. Vaginal douching as a risk factor for acute pelvic inflammatory disease. Obstet Gynecol 1993; 81:601-6.
25. Pittaway DE, Winfield AC, Maxson W, Daniell J, Herbert C, Wentz AC. Prevention of acute pelvic inflammatory disease after hysterosalpingography: efficacy of doxycycline prophylaxis. Am J Obstet Gynecol 1983; 147:623-6.
26. Blackwell AL, Thomas PD, Wareham K, Emery SJ. Health gains from screening for infection of the lower genital tract in women attending for termination of pregnancy. Lancet 1993; 342:206-10.
27. Soper DE. Pelvic inflammatory disease. In: Ransom SB, Dombrowski MB,McNeeley SG, ed. Practical strategies in obstetrics and gynecology. Philadelphia: W.B.Saunders., 2000:65-73.
28. Sexually transmitted diseases treatment guidelines 2002. Centers for Disease Control and Prevention. MMWR Recomm Rep 2002; 51:1-78.
29. Richter HE, Holley RL, Andrews WW, Owen J, Miller KB. The association of interleukin 6 with clinical and laboratory parameters of acute pelvic inflammatory disease. Am J Obstet Gynecol 1999; 181:940-4.
30. Ness RB, Soper DE, Holley RL, et al. Effectiveness of inpatient and outpatient treatment strategies for women with pelvic inflammatory disease: results from the Pelvic Inflammatory Disease Evaluation and Clinical Health (PEACH) Randomized Trial. Am J Obstet Gynecol 2002; 186:929-37.
31. Aboulghar MA, Mansour RT, Serour GI. Ultrasonographically guided transvaginal aspiration of tuboovarian abscesses and pyosalpinges: an optional treatment for acute pelvic inflammatory disease. Am J Obstet Gynecol 1995; 172:1501-3.
32. Nelson AL, Sinow RM, Oliak D. Transrectal ultrasonographically guided drainage of gynecologic pelvic abscesses. Am J Obstet Gynecol 2000; 182:1382-8.